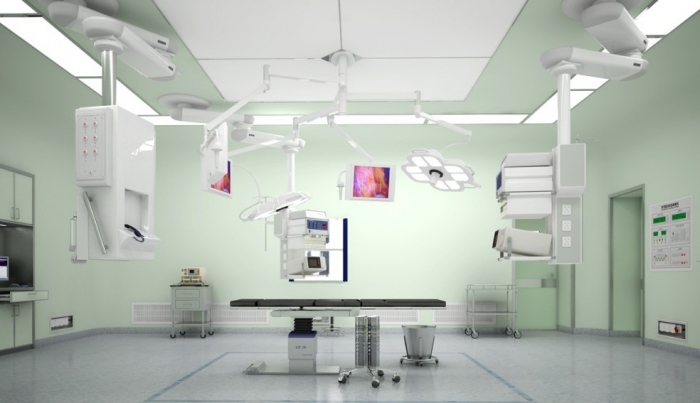
藥物檢測實驗室設計的基本要求
藥物檢查實驗室通常由兩(liang) 個(ge) 部分組成:物理和化學實驗室和微生物實驗室;物理和化學實驗室使用物理和化學。實驗室規劃無菌試驗室-潔淨實驗室-生物安全實驗室的建設方案包括:建築布局和裝修、空氣調節、給排水、氣體(ti) 供應、電氣設計、集中控製、安防、施工工藝、檢測、培訓等多方麵內(nei) 容。實驗室建設不同級別的層流手術室其空氣潔淨度標準不同,例如國內(nei) 標準I級層流手術室的標準為(wei) 潔淨度5級,每立方尺空氣中≥0.5μm的塵粒數,≤100顆或每升空氣中≤3.5 顆。II級層流手術室的標準為(wei) 潔淨度6級,每立方尺空氣中≥0.5μm的塵粒數,≤1000顆或每升空氣中≤35顆。III級層流手術室的標準為(wei) 潔淨度7級,每立方尺空氣中≥0.5μm的塵粒數,≤10000顆或每升空氣中≤352顆。依次類推。實驗室裝修高效安全的手術室空氣淨化係統,保證手術室的無菌環境,可以滿足器官移植、心髒、血管、人工關(guan) 節置換等手術所需的高度無菌環境。采用高效低毒消毒劑,以及合理使用,是保障一般手術室無菌環境的有力措施。
該方法分析和檢驗用於(yu) 生產(chan) 的原材料,包裝材料,中間體(ti) 和成品,並以結果作為(wei) 產(chan) 品是否符合法定要求和內(nei) 部質量標準的依據。微生物實驗室通常具有以下功能:
(1)根據《中國藥典》的要求,進行了微生物試驗方法、無菌試驗、微生物限度試驗、抗生素效價(jia) 微生物試驗、青黴素酶及其活性試驗。
(2)根據現行“藥品生產(chan) 質量管理規範”的要求,采用微生物法測定製藥行業(ye) 潔淨室的潔淨度,並對無菌生產(chan) 區及生產(chan) 過程中需要檢測到的環境進行日常動態監測,如無菌濾池的檢定、環境和設備消毒效果的驗證、無菌藥品包裝密封性驗證中微生物挑戰的驗證等。
3細菌內(nei) 毒素檢查,注射劑的不溶性顆粒檢查。雖然這些測試不是微觀的,但它們(men) 對檢測環境有很高的要求,通常位於(yu) 微生物實驗室。
《藥品生產(chan) 質量管理規範》要求藥品生產(chan) 企業(ye) 負責藥品生產(chan) 全過程的質量管理和檢驗,配備與(yu) 規模相適應的人員、場所、儀(yi) 器設備。藥品生產(chan) 品種及檢驗要求。在微生物實驗室的設計中,應了解檢驗過程、工藝性質、相關(guan) 標準和規範,並根據製藥企業(ye) 的生產(chan) 品種和檢驗工作量安排相應的微生物檢驗功能室。在藥品微生物檢測中,為(wei) 了保證檢測結果的準確性和可靠性,需要對影響微生物檢測的幾個(ge) 因素進行相應的研究。
措施通常如下:
1藥物本身的抑菌作用或藥物中防腐劑的抑菌作用。它們(men) 掩蓋了無菌藥物已被汙染或導致低於(yu) 實際汙染水平的事實。生長比較方法通常用於(yu) 通過在實際測試條件下比較測試樣品存在或不存在下對照測試細菌或陽性細菌的生長來驗證測試方法下測試物品的抑菌作用。
(2)標準品係(試驗品係或陽性品係)的製備、通過、種類及生長狀況應符合現行《中國藥典》的要求。
(3)培養(yang) 基促進細菌生長的能力:培養(yang) 基應具有廣譜,有利於(yu) 樣品中所有活微生物的生長。通過接種不同的實驗細菌並觀察其生長狀態,驗證了培養(yang) 基的敏感性。
4檢查設備,如過濾係統過濾器,過濾材料性能,洗脫液,稀釋劑,中等無菌性和操作程序等,通常采用陰性對照試驗來檢測其影響。
_培養(yang) 條件(溫度、濕度、有氧或無氧)和檢測環境應符合要求。