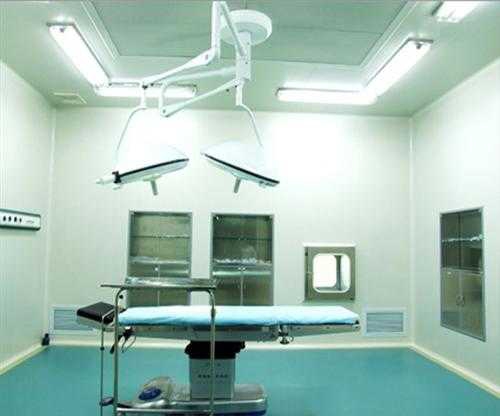
我國醫藥行業(ye) 的《藥品生產(chan) 質量管理規範》(GMP)自從(cong) 1992年頒布以來,已經逐步為(wei) 藥品生產(chan) 企業(ye) 所認識、接受並實施,GMP對於(yu) 企業(ye) 是一項國家強製執行的政策,限期達不到要求的企業(ye) 將停產(chan) 。無菌手術室室高效安全的手術室空氣淨化係統,保證手術室的無菌環境,可以滿足器官移植、心髒、血管、人工關(guan) 節置換等手術所需的高度無菌環境。采用高效低毒消毒劑,以及合理使用,是保障一般手術室無菌環境的有力措施。手術室淨化確保手術台潔淨度達標,一般多采用垂直層流式效果較好 層流手術室是一個(ge) "正壓"環境,其空氣壓力根據其不同區域(如手術間、無菌準備間、刷手間、麻醉間和周圍幹淨區域等)潔淨度不同要求而不同。潔淨手術室按不同專(zhuan) 科,手術間又可分為(wei) 普外、骨科、婦產(chan) 科、腦外科、心胸外科、泌尿外科。燒傷(shang) 科、五官科等手術間。由於(yu) 各專(zhuan) 科的手術往往需要配置專(zhuan) 門的設備及器械,因此,專(zhuan) 科手術的手術間宜相對固定。
GMP認證的核心內(nei) 容是藥品生產(chan) 質量的綜合管理和控製。其內(nei) 容概括為(wei) 軟件管理和硬件設施兩(liang) 部分。硬件設施中的潔淨室是資本密集程度最高的部分之一。清潔工廠建成後,是否符合設計要求,是否符合GMP要求,最終通過檢驗確認。在檢查潔淨室時,一些清潔度測試是不合格的,有些是工廠的一部分,也是整個(ge) 項目的一部分。如果測試失敗,雖然雙方最終都通過整改,調試和清理滿足了要求,但往往浪費了大量的人力物力,延誤了施工期,延誤了GMP認證過程。在測試之前,一些原因和缺陷是完全可以避免的。在我們(men) 的實際工作中,我們(men) 發現不合格清潔度和GMP失效的主要原因和改進措施是:
一、工程設計不合理
這種現象比較少見,主要是在一些小型的淨化級別要求不太高的潔淨室建造上。現在淨化的競爭(zheng) 比較激烈,一些施工單位為(wei) 了得到工程,在投標中給出了較低的報價(jia) 。在後期施工中,利用一些單位不太懂行的情況,偷工減料,使用功率較低的空調通風壓縮機組,使送風功率與(yu) 淨化麵積不匹配,導致潔淨度不合格。還有另外一個(ge) 原因,是使用單位在設計施工開始後,又增加了新的要求和淨化麵積,這也會(hui) 使原先的設計不能達到要求。這種先天性的缺陷是難以改進的,要在工程設計階段避免。
二、用低檔產(chan) 品替代高檔產(chan) 品
在潔淨室高效過濾器的應用上,國家規定在潔淨度10萬(wan) 級或高於(yu) 10萬(wan) 級以上的空氣淨化處理,應采用初效、中效、高效過濾器的三級過濾。而不乏有大型淨化工程在1萬(wan) 級的淨化級別上采用亞(ya) 高效空氣過濾器代替高效空氣過濾器,從(cong) 而造成了潔淨度不合格。最終更換了高效過濾器才符合了GMP認證的要求。
三、送風管或過濾器密封不好
這種現象是施工粗糙造成的,在驗收時會(hui) 表現出在同一係統中某個(ge) 房間或局部不合格,改進的方法是,送風管采用漏光試驗法檢漏,過濾器用粒子計數器對過濾器的斷麵、封膠、安裝框架進行掃描,找出泄露位置,精心密封。
四、回風管道或回風口設計、調試不好
在設計方麵,有時由於(yu) 空間限製,上送風側(ce) 回風或回風出口數量不足,無法使用。在排除了設計原因後,回風出口的調試也是一個(ge) 重要環節。如果調試不好,回風出口阻力過大,回風量小於(yu) 送風量,清潔度也不合格。